近日,我校医药化工学院吴劼/叶盛青教授团队在《chemical science》上发表了题为“access to chiral β-sulfonyl carbonyl compounds via photoinduced organocatalytic asymmetric radical sulfonylation with sulfur dioxide”的研究论文,吴劼教授和叶盛青教授为共同通讯作者。
含有手性中心的磺酰类化合物广泛存在于上市药物分子和生物活性分子中。例如:手性磺酰类药物阿普斯特(apremilast)在临床上用于治疗成人活跃型银屑病关节炎,该药2021年全球年销售额约22亿美元;雷米克林(remikiren)是一类经典的用于治疗高血压的药物;盐酸杜塞酰胺(dorolamide hcl)是在临床上用于青光眼的治疗。据统计,2021年全球销售额前200的小分子药物排行中,磺酰类小分子药物占比约10%,总销售额约250亿美元。由于手性磺酰类小分子化合物在生物医药领域如此重要的地位。因此,发展绿色、高效的合成方法来构建具有生物活性的手性磺酰类分子骨架是目前药物合成和有机合成领域的热点和挑战。
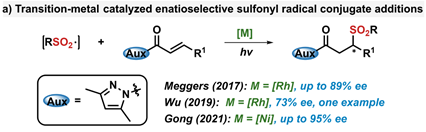
手性β-磺酰取代的羰基化合物作为一类重要的手性磺酰类化合物骨架,其不对称合成主要通过磺酰基亲核试剂对α,β-不饱和羰基化合物的不对称亲核加成实现。近年来,由于自由基物种具有高活性的特点,因此光诱导自由基历程下的不对称亲核加成可以克服传统不对称亲核加成反应在底物活性和空间位阻方面的固有缺陷。同时,自由基的高活性也会带来反应的立体选择性难以控制等挑战。目前已发展的磺酰基自由基对α,β-不饱和羰基化合物的不对称加成反应是基于过渡金属催化的不对称自由基加成。但这类方法都往往要有辅基作为配位导向,不利于底物多样性的拓展。因此,发展新型不对称催化方法来构建手性β-磺酰取代的羰基化合物是该领域的研究难点和热点之一。
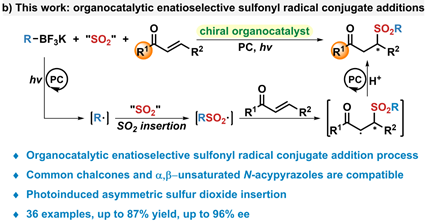
吴劼教授团队近年来一直致力于磺酰药物导向的二氧化硫参与的转化研究,并利用二氧化硫插入策略发展了一系列结构多样的磺酰类化合物的合成方法。该论文在课题组前期的工作基础上,利用光诱导不对称自由基反应,以二氧化硫有机碱络合物为二氧化硫的来源,通过自由基加成途径实现了手性β-磺酰取代的羰基化合物的构建:以烷基氟硼酸钾为原料,在光诱导下产生自由基,随后捕获二氧化硫生成磺酰基自由基,其对α,β-不饱和羰基化合物进行不对称加成,最后经过还原质子化,成功实现了手性β-磺酰取代的羰基化合物的高效立体选择性合成。该方法使用有机小分子催化,有效地解决了过渡金属催化历程下辅基使用的问题。
该项研究工作得到了台州学院、国家自然科学基金、浙江省自然科学基金、浙江省领军型创新团队、金属有机化学国家重点实验室、河南师范大学开放基金的经费支持。
论文链接: